問48(安全性等の調査)は難しい。
問41
一般用医薬品の添付文書に関する記述の正誤について、正しい組み合わせはどれか。
a 「使用上の注意」、「してはいけないこと」及び「相談すること」の各項目の見出しには、それぞれ標識的マークが付されていることが多い。
b 「病気の予防・症状の改善につながる事項」の項目は、必須記載ではない。
c 「消費者相談窓口」の項目には、独立行政法人医薬品医療機器総合機構の担当部門の電話番号、受付時間を記載しなければならない。
d 医薬品の添付文書の内容は、臨時的な改訂を除き、医薬品の有効性・安全性等に係る新たな知見、使用に係る情報に基づき、1年に1回、定期的に改訂される。
a b c d
1 誤 誤 正 正
2 正 誤 誤 正
3 正 正 誤 誤
4 正 正 正 誤
5 誤 正 正 正
一般用医薬品の添付文書に関する問題。
添付文書の改訂に関して「必要に応じて随時改訂」される点は頻出。「毎年改訂」や「定期的に改訂」「1年毎に改訂」ときたら誤り。
a 正しい。R4手引きの改訂により、記述が「統一された標識的マークが付されている」から、「例示された標識的マークが付されていることが多い」に変更されており、正しい記述である。

b 正しい。
c 誤り。製造販売元の製薬企業において購入者等からの相談に応じるための窓口担当部門の名称、電話番号、受付時間等が記載されている。

d 誤り。添付文書の内容は必要に応じて随時改訂がされる。定期的に毎年改訂されるわけではない。
正解・・・3
問42
一般用医薬品の製品表示に関する記述のうち、誤っているものはどれか。
1 医薬品医療機器等法の規定による法定表示のほか、他の法令に基づく製品表示がなされていることがある。
2 適切な保存条件の下で製造後2年を超えて性状及び品質が安定であることが確認されている医薬品には、使用期限の法的な表示義務はない。
3 1回服用量中0.1mL を超えるアルコールを含有する内服液剤(滋養強壮を目的とするもの)については、アルコールを含有する旨及びその分量が記載されている。
4 添付文書を見なくても適切な保管がなされるよう、容器や包装にも保管に関する注意事項が記載されている。
一般用医薬品の製品表示に関する問題。
1 正しい。
2 誤り。×2年⇒○3年
初学者は意外に感じるでしょうが、使用期限については、適切な保存条件の下で製造後3年を超えて性状及び品質が安定であることが確認されている医薬品において法的な表示義務はない。確かに一昔前の漢方薬など、実際に使用期限の書かれていない製品が存在していた。
さらに手引きには「(表示義務はなくても)流通管理等の便宜上、外箱等に記載されるのが通常となっている。」とも書かれており、実際に表示がない製品は稀で、外箱等に記載されるのが通常です。
3 正しい。
4 正しい。
正解・・・2
問43
一般用検査薬に関する記述の正誤について、正しい組み合わせはどれか。
a 添付文書には、「キットの内容及び成分・分量」が記載されており、妊娠検査薬では、専門家による購入者等への情報提供の参考として、検出感度も併せて記載されている。
b 検査結果のみで確定診断はできないので、判定が陽性であれば速やかに医師の診断を受ける旨が、添付文書に記載されている。
c 検査結果が陰性であっても何らかの症状がある場合は、再検査するか又は医師に相談する旨等が、添付文書に記載されている。
d 一般用検査薬は、医薬品副作用被害救済制度の対象とならない。
a b c d
1 正 正 正 誤
2 正 正 誤 正
3 正 誤 正 正
4 誤 正 正 正
5 正 正 正 正
一般用検査薬に関する問題。
第3章で出題される、尿糖・尿タンパク検査薬、妊娠検査薬も合わせて確認を。
a 正しい。
b 正しい。
c 正しい。
d 正しい。
正解・・・5
問44
緊急安全性情報に関する記述の正誤について、正しい組み合わせはどれか。
a 緊急安全性情報は、都道府県知事からの命令、指示、製造販売業者の自主決定等に基づいて作成される。
b A4サイズの黄色地の印刷物で医療機関や薬局等へ直接配布されるものであり、ファックス、電子メールによる情報提供はできない。
c 医薬品及び再生医療等製品について緊急かつ重大な注意喚起や使用制限に係る対策が必要な状況にある場合に作成されるが、医療機器については作成の対象とならない。
d 一般用医薬品に関係する緊急安全性情報が発出されたことはない。
a b c d
1 誤 誤 誤 正
2 誤 誤 正 誤
3 誤 正 誤 誤
4 正 誤 誤 誤
5 誤 誤 誤 誤
今回は緊急安全性情報(イエローレター)に関する出題だが、安全性速報(ブルーレター)との違いはしっかり区別できるようにセット学習を。
a 誤 緊急安全性情報は、厚生労働省からの命令、指示、製造販売業者の自主決定等に基づいて作成される。
b 誤 製造販売業者から医療機関や薬局等への直接配布のほか、ダイレクトメール、ファックス、電子メール等による情報提供(1ヶか月以内)等により情報伝達される。
c 誤 医薬品、再生医療等製品だけでなく、医療機器についても作成の対象となる。
d 誤 小柴胡湯による間質性肺炎に関する緊急安全性情報(平成8年3月)のように、一般用医薬品にも関係する緊急安全性情報が発出されたこともある。
正解・・・5
問45
医薬品医療機器等法第68条の10第2項の規定に基づき、登録販売者が行う医薬品の副作用等報告に関する記述の正誤について、正しい組み合わせはどれか。
a 医薬品の副作用等によるものと疑われる健康被害の発生を知った場合において、保健衛生上の危害の発生又は拡大を防止するため必要があると認めるときは、その旨を15日以内に報告しなければならないと定められている。
b 安全対策上必要があると認めるときは、医薬品の過量使用や誤用等によるものと思われる健康被害についても、報告がなされる必要がある。
c 医薬品との因果関係が必ずしも明確でない場合であっても、報告の対象となり得る。
d 報告者に対しては、安全性情報受領確認書が交付される。
a b c d
1 正 正 正 誤
2 正 正 誤 正
3 正 誤 正 正
4 誤 正 正 正
5 正 正 正 正
毎年出題されている医薬品・医療機器等安全性情報報告制度に関する問題。
なお、この制度による報告は、登録販売者を含む医療関係者にとって「義務」である。(但し、実際にはあまり報告されていないが・・)

a 誤り。報告期限は特に定められていないが、報告の必要性を認めた場合においては、適宜速やかに、報告書を総合機構に送付することとされている
b 正しい。
c 正しい。
d 正しい。
正解・・・4
問46
独立行政法人医薬品医療機器総合機構(以下「総合機構」という。)に関する記述の正誤について、正しい組み合わせはどれか。
a 総合機構のホームページでは、添付文書情報のほか、医薬品等の製品回収に関する情報や患者向医薬品ガイド等の情報が掲載されている。
b 医薬品副作用被害救済制度において、健康被害を受けた本人(又は家族)の給付請求を受けて、その健康被害が医薬品の副作用によるものかどうかなど、医学的薬学的判断を要する事項について総合機構が審議し、給付の判定を行っている。
c 総合機構は、医薬品医療機器情報配信サービス(PMDAメディナビ)を行っており、このサービスは誰でも利用可能である。
d 総合機構は、医薬品副作用被害救済制度の相談窓口を設けている。
a b c d
1 誤 正 正 誤
2 正 誤 正 正
3 誤 正 誤 正
4 正 誤 正 誤
5 正 正 誤 正
独立行政法人医薬品医療機器総合機構に関する問題。
a 正しい。
b 誤り。医学的薬学的判断を要する事項について薬事・食品衛生審議会の諮問・答申を経て、厚生労働大臣が判定した結果に基づいて、各種給付が行われる。
c 正しい。
d 正しい。
正解・・・2
問47
医薬品副作用被害救済制度の救済給付に関する記述のうち、正しいものはどれか。
1 医療手当の給付は、請求に係る医療が行われた日の属する月の翌月の初日から10年以内に請求を行う必要がある。
2 障害児養育年金は、医薬品の副作用により一定程度の障害の状態にある20歳未満の人を養育する人に対して給付されるものである。
3 葬祭料の給付は、請求期限がない。
4 遺族年金の給付は、請求期限がある。
医薬品副作用被害救済制度に関する問題。
給付の種類としては、医療費、医療手当、障害年金、障害児養育年金、遺族年金、遺族一時金及び葬祭料があるが、全て細かく憶えようとすると結構大変である。
出題ポイントとしては、給付の請求の期限、定額がどうかが問われる事が多い。
詳細に憶える時間がなければ、最低限以下のポイントは押さえておきたい。
請求の期限なし・・・障害年金、障害時養育年金
請求の期限・・・(〇〇から)5年以内
給付額が定額ではない・・・医療費
なお、障害年金は18歳以上の障害が残った人に支払われるもの、障害児養育年金は、18歳未満の障害の残った方を養育する人に支払われるものである。
また、請求の期限は、様々な例外条件も書かれているが、とりあえず「5年以内」で最低限憶えておく。
1 誤り。×10年以内⇒○5年以内
2 誤り。×20歳未満⇒○18歳未満
3 誤り。葬祭料の給付は請求期限がある。
4 正しい。
正解・・・4
問48
医薬品の製造販売業者等が行う安全性等の調査に関する記述の正誤について、正しい組み合わせはどれか。
a 既存の医薬品と明らかに異なる有効成分が配合されたものについては、10年を超えない範囲で厚生労働大臣が承認時に定める一定期間(概ね8年)、承認後の使用成績等を製造販売業者等が集積し、厚生労働省へ提出する制度(再審査制度)が適用される。
b 製造販売業者等には、医薬品医療機器等法第68条の10第1項の規定に基づき、製造販売をし、又は承認を受けた医薬品について、その副作用により、癌その他の重大な疾病、障害若しくは死亡が発生するおそれがあることを示す研究報告を知ったときは、その旨を30日以内に厚生労働大臣に報告しなければならない。
c 医療用医薬品で使用されていた有効成分を一般用医薬品で初めて配合したものについては、承認条件として承認後の一定期間(概ね3年)、安全性に関する調査及び調査結果の報告が求められている。
d サリドマイド事件、スモン事件等を踏まえ、1979年に薬事法が改正され、医薬品の市販後の安全対策の強化を図るための再審査・再評価制度等が創設された。
a b c d
1 正 正 正 誤
2 正 正 誤 正
3 正 誤 正 正
4 誤 正 正 正
5 正 正 正 正
医薬品の製造販売業者等が行う安全性等の調査に関する問題。
数値の正誤判断が多くあり、難易度は高い。
a 正しい。
医薬品の再審査制度に関する問題だが、既存の医薬品と明らかに異なる有効成分(いわゆるダイレクトOTC)が配合されたものについては、10年を超えない範囲で厚生労働大臣が承認時に定める一定期間(概ね8年)、承認後の使用成績等を製造販売業者等が集積し、厚生労働省へ提出する制度(再審査制度)が適用される。
↑なお、具体的としては、発毛剤のリアップ(ミノキシジル)をイメージしてもらえればOKです。
b 正しい。
企業からの副作用症例・感染症症例の報告に関する問題だが、ポイントとして、その重篤性と予測性から、報告期限は「15日以内」「30日以内」、さらに「定期報告」があることは押さえておく。試験対策の第一歩として、とりあえず「死亡した事例」は「15日以内」と憶えてしまって良いでしょう。
そして、今回出題されている、(副作用・感染症等に関する)「研究報告」の報告期限は「30日以内」となっている。
c 正しい。
医療用医薬品で使用されていた有効成分を要指導医薬品・一般用医薬品で初めて配合したもの(いわゆるスイッチOTC)については、承認条件として承認後の一定期間(概ね3年)、安全性に関する調査及び調査結果の報告が求められている。
↑最近のものだと、花粉症向けのアレグラFX(フェキソフェナジン)やロキソニンS(ロキソプロフェン)をイメージしてもらればOKです。

d 正しい。なお、サリドマイド事件、スモン事件等を踏まえ、併せて医薬品副作用被害救済制度も創設されたことも押さえておこう。
正解・・・5
問49
医薬品医療機器等法第68条の10第2項の規定に基づく医薬品の副作用等報告について、医薬品安全性情報報告書の報告様式にある項目として、誤っているものはどれか。
1 患者氏名
2 性別
3 体重
4 既往歴
5 過去の副作用歴
手引き第5章別紙にある、「医薬品安全性情報報告書」を見て確認しておこう。
「患者氏名」ではなく、「患者イニシャル」を記載する様式になっている。
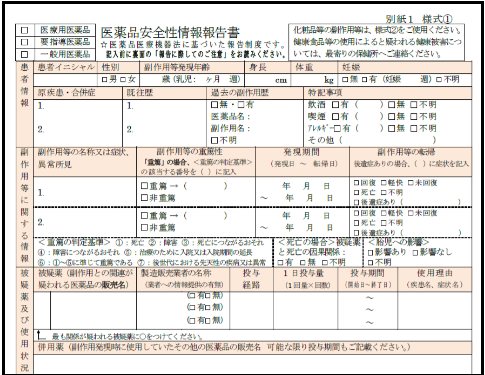
正解・・・1
問50
一般用医薬品の安全対策に関する記述について、( )の中に入れるべき字句の正しい組み合わせはどれか。
日本では2003年8月までに、( a )が配合された一般用医薬品による脳出血等の副作用症例が複数報告され、それらの多くが用法・用量の範囲を超えた使用又は禁忌とされている( b )患者の使用によるものであった。そのため、厚生労働省から関係製薬企業等に対して、使用上の注意の改訂、情報提供の徹底等を行うとともに、代替成分として( c )等への速やかな切替えにつき指示がなされた。
a b c
1 塩酸フェニルプロパノールアミン 高血圧症 プソイドエフェドリン塩酸塩
2 塩酸フェニルプロパノールアミン 糖尿病 ジヒドロコデインリン酸塩
3 ジヒドロコデインリン酸塩 高血圧症 プソイドエフェドリン塩酸塩
4 プソイドエフェドリン塩酸塩 糖尿病 ジヒドロコデインリン酸塩
5 プソイドエフェドリン塩酸塩 高血圧症 塩酸フェニルプロパノールアミン
塩酸フェニルプロパノールアミン(PPA)含有医薬品に関する問題。
安全対策に関する問題では、小柴胡湯による間質性肺炎と並び、第5章頻出なので絶対落とさないように。
代替成分のプソイドエフェドリン塩酸塩は、第3章、5章ともに超頻出成分です。
a 塩酸フェニルプロパノールアミン
b 高血圧症
c プソイドエフェドリン塩酸塩
正解・・・1

