H28 福岡県(九州・沖縄) 第5章 医薬品の適正使用・安全対策(問41-50)
頻出のポイントばかり。特別難しい問題はない。
問41 一般用医薬品の添付文書に関する以下の記述のうち、誤っているものを一つ選びなさい。
1 医薬品の有効性・安全性等に係る新たな知見、使用に係る情報に基づき、定期的に改訂がなされている。
2 重要な内容が変更された場合には、改訂年月を記載するとともに改訂された箇所を明示することとされている。
3 添付文書の販売名の上部に、添付文書の必読及び保管に関することが記載されている。
4 一般用医薬品を使用した人が医療機関を受診する際、その添付文書を持参し、医師や薬剤師に見せて相談がなされることが重要である。
一般用医薬品の添付文書に関する問題。
1 誤り。今まで何度も登場しているひっかけ問題。×定期的に改訂→〇必要に応じて随時改訂
2 正しい。
3 正しい。

4 正しい。実際に行われることは殆どないが、正しい内容である。
正答・・・1
問42 一般用医薬品の添付文書に関する以下の記述の正誤について、正しい組み合わせを下から一つ選びなさい。
ア 「服用前後は飲酒しないこと」等の小児では通常当てはまらない内容は、小児に使用される医薬品の添付文書に、その医薬品の配合成分に基づく一般的な注意事項として記載されていない。
イ 使用上の注意は、「してはいけないこと」、「相談すること」及び「その他の注意」から構成され、 適正使用のために重要と考えられる項目が前段に記載されている。
ウ 「してはいけないこと」には、守らないと症状が悪化する事項、副作用又は事故等が起こりやすくなる事項について記載されている。
エ 副作用については、まれに発生する重篤な副作用について副作用名ごとに症状が記載され、そのあとに続けて、一般的な副作用について発現部位別に症状が記載されている。
ア イ ウ エ
1 正 正 正 正
2 正 誤 正 誤
3 誤 正 正 誤
4 誤 正 誤 誤
5 誤 誤 誤 正
一般用医薬品の添付文書に関する問題。
ア 誤り。
イ 正しい。

ウ 正しい。

エ 誤り。先にまず一般的な副作用について発現部位別に症状が記載され、そのあとに続けて、まれに発生する重篤な副作用について副作用名ごとに症状が記載される。

正答・・・3
問43 一般用医薬品の添付文書に関する以下の記述のうち、誤っているものを一つ選びなさい。
1 用法及び用量については、年齢区分、1回用量、1日の使用回数等について一般の生活者に分かりやすく、表形式で示されるなど工夫して記載されている。
2 小児における使用に関して認められていない年齢区分がある場合は、当該年齢区分に当たる小児に使用させない旨が記載されている。
3 効能又は効果に関連する注意事項がある場合は、効能又は効果の項目に続けて、これと区別して記載されている。
4 有効成分が不明な場合は、成分及び分量の項目について記載の必要がない。
一般用医薬品の添付文書に関する問題。
1 正しい。
2 正しい。例えばインドメタシン配合の湿布薬には、「してはいけないこと」の欄に「11未満の小児」が記載されている。

3 正しい。
4 誤り。
正答・・・4
問44 一般用医薬品の保管及び取扱い上の注意に関する以下の記述のうち、誤っているものを一つ選びなさい。
1 誤用の原因になったり、適切な品質を保持できなくなったりするおそれがあるため、他の容器に入れ替えない。
2 家庭内では、小児が容易に手に取れる場所や、小児の目につくところに保管しない。
3 点眼薬は、複数の使用者間で使い回されると、万一、使用に際して薬液に細菌汚染があった場合に、別の使用者に感染するおそれがあるため、他の人と共用しない。
4 錠剤や散剤は変質を避けるため、冷蔵庫内に保管することが望ましい。
一般用医薬品の保管及び取扱い上の注意に関する問題。
これは簡単。1~3は常識的に判断できるでしょう。
1 正しい。
2 正しい。
3 正しい。
4 誤り。錠剤や散剤、カプセル剤は、取り出したときに室温との急な温度差で湿気を帯びるおそれがあるため、冷蔵庫内での保管は不適当である。
正答・・・4
問45 製品表示に関する以下の記述の正誤について、正しい組み合わせを下から一つ選びなさい。
ア 1回服用量中0.1mLを超えるアルコールを含有する内服液剤(滋養強壮を目的とするもの) については、アルコールを含有する旨及びその分量が記載されている。
イ 添付文書に記載されている使用上の注意「してはいけないこと」の項において、副作用や事故等が起きる危険性を回避するために記載されている内容については、外部の容器又は被包に記載されている。
ウ 使用期限の表示については、適切な保存条件の下で製造後2年を超えて性状及び品質が安定であ ることが確認されている医薬品において法的な表示義務はない。
エ 表示された「使用期限」は、開封、未開封に関わらず、品質が保持される期限である。
ア イ ウ エ
1 正 正 正 正
2 正 正 誤 誤
3 正 誤 誤 正
4 誤 正 誤 正
5 誤 誤 正 誤
製品表示に関する問題。
1 正しい。
2 正しい。
3 誤り。×2年→〇3年。初めて学習する受験生は意外に感じるかと思うが、使用期限について適切な保存条件の下で製造後3年を超えて性状及び品質が安定であることが確認されている医薬品において法的な表示義務はない。確かに一昔前の漢方薬など、実際に使用期限の書かれていない製品が存在していた。
さらに手引きには「(表示義務はなくても)流通管理等の便宜上、外箱等に記載されるのが通常となっている。」と書かれている。
流通管理はもちろんのこと、今の時代に使用期限の書いていないような商品は消費者が敬遠するので、実際には使用期限の記載のない製品は殆どないのが現状である。
4 誤り。表示された「使用期限」は、あくまで未開封状態で保管された場合に品質が保持される期限である。
正答・・・2
問46 以下の記述について、( )の中に入れるべき字句の正しい組み合わせを下から一つ選びなさい。
( ア )は、医薬品、医療機器又は再生医療等製品について緊急かつ重大な注意喚起や使用制限に係る対策が必要な状況にある場合に、厚生労働省からの命令、指示、製造販売業者の自主決定等に基づいて作成される、A4サイズの( イ )地の印刷物である。
ア イ
1 緊急安全性情報 黄色
2 安全性速報 黄色
3 緊急安全性情報 赤色
4 安全性速報 赤色
5 緊急安全性情報 青色
緊急安全性情報(イエローレター)、安全性速報(ブルーレター)に関する問題。
これは簡単。「緊急かつ重大」から、緊急安全性情報の方を容易に選べるでしょう。
正答・・・1
問47 医薬品の安全性情報及び適正使用情報に関する以下の記述のうち、誤っているものを一つ選びなさい。
1 一般用医薬品に関係する緊急安全性情報が発出されたことはない。
2 独立行政法人医薬品医療機器総合機構(以下「総合機構」という。)による医薬品医療機器情報配信サービス(PMDAメディナビ)は誰でも利用可能であり、最新の情報を入手することができる。
3 総合機構の「医薬品医療機器情報提供ホームページ」において、医療用医薬品及び医療機器のほか、要指導医薬品及び一般用医薬品についても添付文書情報を掲載している。
4 厚生労働省においては、医薬品(一般用医薬品を含む)、医療機器等による重要な副作用、不具合等に関する情報をとりまとめ、「医薬品・医療機器等安全性情報」として、広く医薬関係者向けに情報提供を行っている。
医薬品の安全性情報及び適正使用情報に関する問題。
1 誤り。これは良く問われている内容。一般用医薬品でも関係する緊急安全性情報が発出されたことがある。小柴胡湯による間質性肺炎に関する緊急安全性情報(平成8年3月)は是非憶えておく。
2 正しい。PMDAメディナビは、誰でも利用可能である。

3 正しい。医薬品医療機器情報提供ホームページについては、出来れば実際にサイトも覗いておこう。
4 正しい。医薬品・医療機器等安全性情報では、広く医薬関係者向けに情報提供を行っている。「医薬品医療機器情報提供ホームページ」や、医学・薬学関係の専門誌等にも転載されている。

正答・・・1
問48 副作用情報等の収集に関する以下の記述のうち、誤っているものを一つ選びなさい。
1 医薬品・医療機器等安全性情報報告制度は、医薬品の使用、販売等に携わり、副作用等が疑われる事例に直接対応する医薬関係者からの情報を広く収集することによって、医薬品の安全対策のより着実な実施を図ることを目的としている。
2 医師や薬剤師等の医薬関係者による副作用等の報告は義務化されたが、その医薬関係者に登録販売者は含まれていない。
3 製造販売業者等には、医薬品医療機器等法第68条の10第1項の規定に基づき、その製造販売をし、又は承認を受けた医薬品について、その副作用等によるものと疑われる健康被害の発生、その使用によるものと疑われる感染症の発生等を知ったときは、その旨を定められた期限までに厚生労働大臣に報告することが義務づけられている。
4 薬局開設者、医療施設の開設者、医薬品の販売業者又は医師、歯科医師、薬剤師その他の医薬関係者においては、医薬品医療機器等法第68条の2第2項により、製造販売業者等が行う情報収集に協力するよう努めなければならない。
副作用情報等の収集、医薬品・医療機器等安全性情報報告制度に関する問題。

1 正しい。
2 誤り。「薬局開設者、病院、診療所若しくは飼育動物診療施設の開設者又は医師、歯科医師、薬剤師、登録販売者、獣医師その他の医薬関係者」に義務化されており、当然「登録販売者」も含まれている。なお、平成28年の東京・南関東地区の問題では、獣医師や薬局開設者にも義務があるかが問われていた。
3 正しい。
4 正しい。
正答・・・2
問49 医薬品の副作用情報の評価及び措置に関する以下の記述について、( )の中に入れるべき字句の正しい組み合わせを下から一つ選びなさい。
医薬品医療機器等法第68条の10の規定に基づき、収集された副作用情報については、独立行政法人医薬品医療機器総合機構において( ア )の意見を聴きながら調査検討が行われ、その結果に基づき、厚生労働大臣は、( イ )の意見を聴いて、使用上の注意の改訂の指示等を通じた 注意喚起のための情報提供や、効能・効果や用法・用量の一部変更、調査・実験の実施の指示、製造・ 販売の中止、製品の回収等の安全対策上必要な行政措置を講じている。
ア イ
1 専門委員 日本製薬団体連合会
2 薬事・食品衛生審議会 日本製薬団体連合会
3 日本製薬団体連合会 薬事・食品衛生審議会
4 薬事・食品衛生審議会 専門委員
5 専門委員 薬事・食品衛生審議会
医薬品の副作用情報の評価及び措置に関する問題。
今までそれ程問われいていないが憶えておく。
ア 専門委員
イ 薬事・食品衛生審議会
正答・・・5
問50 医薬品による副作用等が疑われる場合の報告に関する以下の記述のうち、正しいものの組み合わせを下から一つ選びなさい。
ア 報告の必要性を認めた場合においては、医薬品医療機器等法第68条の13第3項に基づき、情報を入手してから1週間以内に、郵送、ファクシミリ又は電子メールにより、報告書を独立行政法人医薬品医療機器総合機構(以下「総合機構」という。)に送付しなければならない。
イ 報告様式は、総合機構のホームページから入手できる。
ウ 医薬品との因果関係が必ずしも明確でない場合であっても報告の対象となり得る。
エ 情報の正確性を確保するため、報告様式の記入欄すべてに記入しなければならない。
1(ア、ウ) 2(ア、エ) 3(イ、ウ) 4(イ、エ)
副作用情報等の収集、医薬品・医療機器等安全性情報報告制度に関する問題。
医薬品による副作用等が疑われる場合の報告に関する問題。
1 誤り。×1週間以内に→報告期限は定められていない。なお「郵送、ファクシミ、電子メール」はどれでもOK。
2 正しい。↓実際に、HPから入手した報告様式
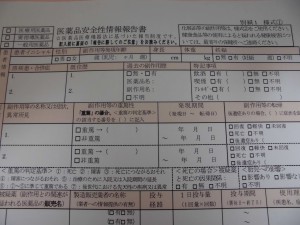
3 正しい。これも良く問われている内容。
4 誤り。報告様式の記入欄すべてに記入がなされる必要はない。
正答・・・3
(Visited 1,667 times, 1 visits today)
